生物医用电极作为一种能够有效地将生物体电化学活动产生的离子电位转换成测量系统电子电位的传感器,广泛应用于现代临床检测和生物医学测量中。近年来,由于生物医用电极在心电图ECG、脑电图EEG、肌电图EMG以及电阻抗成像EIT等领域的广泛应用,新的生物医用电极结构及高效低成本的制造方法不断涌现,制造技术获得飞速发展。本篇文章将带大家简单了解下常见生物医用电极种类及其制造技术。
Ag/AgCI电极
Ag/AgCl电极是生物电检测技术中广泛使用的一种生物医用电极,一般是由电极芯、Ag/AgCl层、导电凝胶、无纺布等部件组成。一般而言,Ag/AgCl层通常采用电镀/电解等加工工艺形成。
目前,在生物电信号检测技术中,Ag/AgCl电极不仅能够在较低电流条件下将离子电流转换成电子电流,且具有电信号基线稳定、抗干扰能力强、制造与使用较为方便、价格便宜、易于生产等优点,在心电、脑电等测量中获得非常广泛的应用。

图1 柏医自主研发皮下植入式微针型Ag/AgCl电极
由于导电凝胶的存在,Ag/AgCl电极在使用过程中容易发生脱水干燥,使得导电凝胶的电特性发生某些变化,不能够长期连续使用。由于导电凝胶的电阻抗不稳定性,在高精度实验中容易引入较大的噪声和误差,从而导致测量结果的不够精确。同时,实验前需要一定的准备时间,需对皮肤进行处理,尽可能擦除皮肤表面的角质层。此外,导电凝胶还有可能会引起皮肤过敏反应,产生红肿等现象。柏医研发的Ag/AgCl电极,属于干电极,工艺简单,易于批量制造,正在推进相关产业化应用。
微针电极
微针技术一般是指通过微细制造方法在硅材料、金属、聚合物和玻璃等材料表面,采用化学刻蚀工艺、反应等离子刻蚀等手段形成的阵列式微针结构。一般而言,单个微针结构的尺寸通常是直径为30~80um,长度100um以上。

图2 柏医自主研发的硅基微针阵列电极
微针电极设计要考虑到皮肤的分层结构,需要刺穿角质层(厚度一般为1015um),刺入导电表皮层(厚度一般为50100um),以避开角质层的高阻抗特性,同时还不能刺到真皮层(包括神经和血管)以避免对皮肤造成损伤,从而导致疼痛和出血等现象。因此,微针刺入深度应该大于1015um,小于50100um,使其在角质层上产生一个无痛的电极-电解液界面,并把活性细胞引起离子流转化成电子电流。
与传统的Ag/AgCl生物电位电极比较,微针电极往往不需要皮肤准备和电解凝胶,使用较为方便可靠,具有更小的阻抗,有较小的电化学噪声,更有利于长期测量使用。
柔性衬底电极
柔性衬底电极由于可以实现与人体组织,特别是与皮肤的高度贴合,并可以满足人体不同部位的穿戴要求,应用范围非常广泛,已成为当生物医用体表电极的重要研究方向。目前,可用于柔性衬底电极材料主要有聚二甲基硅氧烷(PDMS)、聚酰亚胺(PI)、聚对苯二甲酸乙二醇酯(PET)等。

图3 柏医自主研发的柔性衬底电极
在应用方面,柏医研发的持续血糖监测系统通过表面金属化、MEMS图案化工艺,实现4mm电极制备,比目前市面上流行的5mm电极短了20%,兼具高精度及低成本特性,具有知识产权自主可控、工艺简单、响应快速、稳定性好、准确性高等优点。

图4 柏医自主研发的持续血糖监测系统
绝缘干电极
绝缘干电极与上述电极的工作原理都不一样,绝缘干电极是利用很薄的绝缘膜把金属电极与人体隔开,在人体和金属电极之间形成电容,人体和电极片则分别为电容的2个极片,中间的绝缘膜为电容器的中间介质,生物电信号可以通过这一特殊的电容器耦合到缓冲放大器输入端,实现对生物电位变化的测量。目前,绝缘干电极在航空航天、水下作业、生物医学测量等领域的信号的检测中获得了广泛的应用。

图5 绝缘干电极应用在心电测量过程
在应用方面,柏医生物传感器生态圈合作伙伴杭州祺福医疗科技有限公司(以下简称“祺福医疗”)将绝缘干电极技术与柔性电路设计、通讯传输、柔性印刷电路板工艺相结合,研制可穿戴柔性化脑电传感系统,大幅降低界面阻抗,显著提高了传感器的抗运动干扰能力,提高了穿戴式脑电检测的信噪比和稳定性,并成功用于临床条件下的精确检测视觉和听觉诱发脑电信号以及纤维性房颤、中风等患者的脑电、心电等电生理特征。
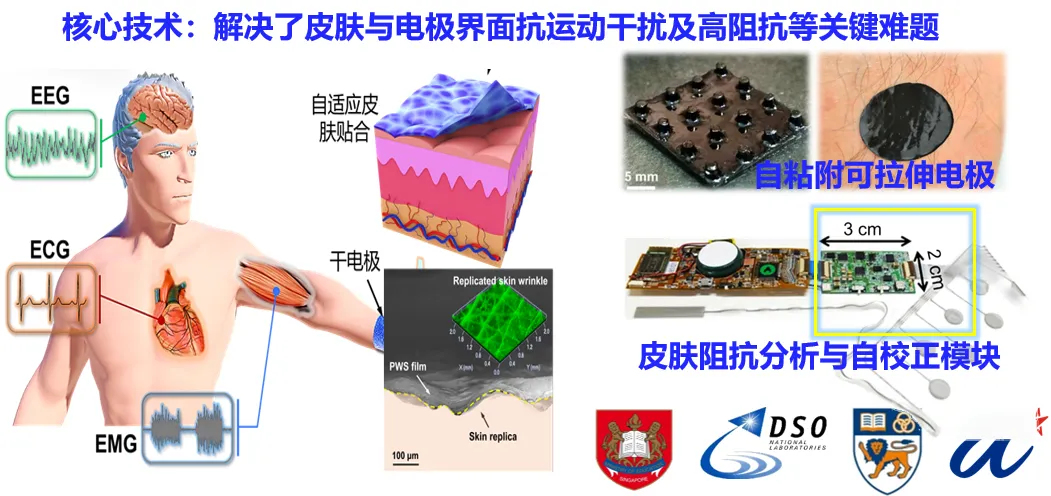
图6 柏医合作伙伴祺福医疗将绝缘干电极技术应用在柔性可穿戴脑电传感器开发中
柏医生物电极解决方案
柏医研发的柔性电化学电极具备工艺简单、电化学性能稳定、批量一致性高等优势。无论是平面电极、微针电极都可以相近的工艺完成,灵活高效。公司研发的标准电极具备如下特性:1.PI/LCP柔性基材,厚度规格:50um/75um/100um/125um/150um/175um等;2.单层双面两电极体系;3.外形可定制,支持切片。

图7 柏医主要的生物电极产品
参考文献:
[1] 周伟, 刘伟, 邱清富, 等. 生物医用电极制造技术及应用研究进展. 科学通报, 2015, 60: 1352–1360.
[2] Geddes L A, Valentinuzzi M E. Temporal changes in electrode impedance while recording the electrocardiogram with dry electrodes. Ann Biomed Eng, 1973, 1: 356–367.
[3] Lin C T, Ko L W, Chiou J C, et al. Noninvasive neural prostheses using mobile and wireless EEG. Proc IEEE, 2008, 96: 1167–1183.
[4] Searle A, Kirkup L. A direct comparison of wet, dry and insulating bioelectric recording electrodes. Physiol Meas, 2000, 21: 271–283.
[5] Baek J Y, An J H, Choi J M, et al. Flexible polymeric dry electrodes for the long-term monitoring of ECG. Sensor Actuat A, 2008, 143: 423–429.
[6] 刘冉, 王晓浩, 周兆英, 等. MEMS微针阵列及其在生物医学上的应用. 生物医学工程学杂志, 2004, 21: 482–485.
[7] Moon J H, Baek D H, Choi Y Y, et al. Wearable polyimide-PDMS electrodes for intrabody communication. J Micromech Microeng, 2010, 20: 025032.
[8] Jung H C, Moon J H, Baek D H, et al. CNT/PDMS composite flexible dry electrodes for long-term ECG monitoring. IEEE Trans Bio-Med Eng, 2012, 59: 1472–1479.
版权申明:
本网站所有原创作品,其版权属于本网站所有。其他媒体、网站或个人转载使用时不得进行商业性的原版原式的转载,也不得歪曲和篡改本网站所发布的内容。如转载须注明文章来源:杭州柏医健康科技有限公司网站。